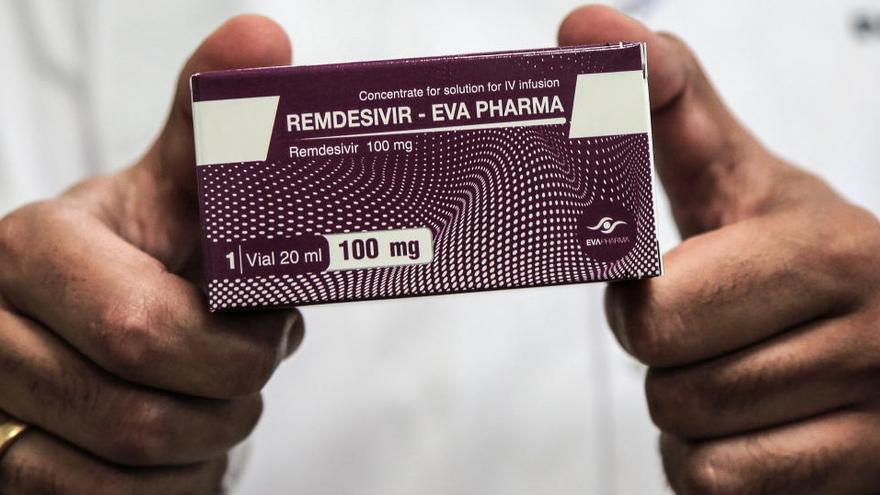
La farmacéutica estadounidense Gilead anunció este lunes que va a vender su fármaco Remdesivir, el primero que se ha mostrado efectivo para tratar la COVID-1para los Gobiernos de países desarrollados, lo que elevaría el precio del tratamiento más habitual a 2.082 euros por paciente y el de las terapias más largas a 3.818 euros.
En el caso de los países en vías de desarrollo, Gilead indicó que ha alcanzado varios acuerdos con productores de medicamentos genéricos para poder ofrecer el tratamiento a un precio más reducido y facilitar acceso a él en todo el mundo.
En Estados Unidos, desde que en mayo se aprobó de emergencia el uso de Remdesivir para enfermos de coronavirus, los hospitales han estado usando dosis donadas por Gilead, que a partir de julio comenzará a cobrar por el medicamento.
En su país, Gilead ha decidido fijar el mismo precio de 390 dólares por vial para los programas de sanidad pública como Medicare, mientras que para los privados -los más habituales en Estados Unidos- será de 462,9 euros, lo que supone un precio de 2.777 para el tratamiento más habitual, que consta de seis dosis, y de 5.091 euros para el más largo, mucho menos común.
El precio superior para los programas privados se deriva de que habitualmente en EEUU los programas públicos reciben descuentos en los medicamentos con respecto al precio del mercado.
En una carta abierta, la empresa explicó que quería evitar negociar el precio del Remdesivir país por país y asegura que lo fijó teniendo en cuenta la situación de los países desarrollados con menos capacidad adquisitiva y claramente "por debajo" del valor que el medicamento ofrece.
Según Gilead, estudios han mostrado que de media los pacientes tratados con este fármaco pasan hospitalizados cuatro días menos, lo que supone un importante ahorro para los centros.
El Remdesivir, una terapia experimental que empezó a desarrollarse en 2009 y se puso a prueba con pacientes del ébola a mediados de la década pasada, se ha autorizado de emergencia para el coronavirus SARS-CoV-2 porque un ensayo clínico estadounidense mostró que ese fármaco acorta el tiempo de recuperación en algunos pacientes.
En Europa, la Agencia Europea del Medicamento (EMA) recomendó autorizar el medicamento para el tratamiento de la COVID-19 en adultos y adolescentes de más de 12 años con neumonía.
El Remdesivir es un antiviral que ralentiza la producción de nuevas partículas de virus y, como resultado, una infección viral se desarrolla con menos rapidez y los pacientes en estado grave se recuperan una media de cuatro días antes de lo habitual, según un amplio estudio llevado a cabo en Estados Unidos.
"No es la panacea"
Por su parte, el director del Centro de Coordinación de Alertas y Emergencias Sanitarias, Fernando Simon, ha reconocido que el tratamiento con el medicamento Remdesivir "tiene algún efecto en la reducción" del tiempo de padecimiento del coronavirus y, por lo tanto, "ayuda", pero ha recalcado que "no es la panacea".
Fernando Simón ha señalado que el Remdesivir produce "algún efecto" en la reducción de las complicaciones que puede producir la COVID-19, así como el tiempo de la enfermedad. "No es la panacea, es un fármaco más que ayuda", ha continuado Simón, quien ha confiado en que la investigación del coronavirus permita que se descubra un medicamento "más eficaz" que acabe con la enfermedad. "Probablemente surjan otros en las próximas semanas", ha dicho.
"No podemos considerarlo como el tratamientos que nos va a solucionar el problema", ha insistido el director del Centro de Coordinación de Alertas y Emergencias Sanitarias quien, sin embargo, ha recalcado que "es una ayuda más".
Simón se ha referido asimismo al estudio de la Universidad de Barcelona que detecta la presencia del SARS-CoV-2 en muestras de aguas residuales recogidas en Barcelona el 12 de marzo de 2019, lo que significa que estaba presente un año antes de que se declarara la pandemia de coronavirus a nivel mundial (11 de marzo de 2020) y se decretara el estado de alarma en España (14 de marzo de 2020).
Ha recordado que Sanidad participa "de forma intensa" a través del Instituto de Salud Carlos III en ese estudio al que, sin embargo, no ha tenido acceso aún, por lo que prefiere ser "precavido". Sin embargo, ha hecho hincapié en que el hecho de que "hace un año y pico se planteara que había circulación del virus en Barcelona es cuando menos algo que hay que discutir".